SUSTITUCIÓN
NUCLEOFÍLICA ACÍLICA
Las sustancias que sufren la denominada sustitución nucleofílica acílica son los denominados derivados de los ácidos carbóxílicos, que incluyen amidas, ésteres, tioésteres, anhidridos de ácido y haluros de acilo.
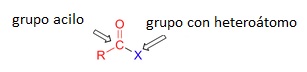
Los derivados de los ácidos carboxílicos se diferencias de los aldehidos y las cetonas porque el carbono carbonílico está unido a un grupo que contiene un heteroátomo. Un derivado de ácido tiene dos zonas diferenciadas: por una parte la cadena alquilo junto al grupo carbonilo forman el GRUPO ACILO, por otra parte, el heteroátomo y su grupo. Este último no es más que la forma desprotonada de otro grupo funcional, por ejemplo, RO- de los ésteres es la forma desprotonada de un alcohol ROH, o -NR2 es la forma desprotonada de una amina HNR2.
SUSTITUCIÓN NUCLEOFÍLICA ACÍLICA
La sustitución nucleofílica acílica se produce en dos etapas:
1.- Ataque del nucleófilo
El nucleófilo ataca al carbono carbonílico, deficitario electrónicamente. Como resultado de este ataque se produce la unión del nucleófilo al carbono, dando lugar a un intermedio de reacción tetracoordinado. Para que ello ocurra, el carbono ha tenido que modificar su hibridación de sp2 a sp3.
2.- Expulsión del grupo del heteroátomo
En ese punto, el intermedio tetraédrico colapsa se vuelve a formar el doble enlace entre el carbono y el oxígeno y el grupo del heteroátomo es expulsado como grupo saliente.
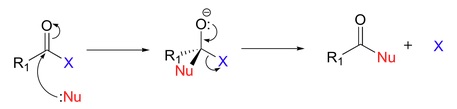
El efecto neto de la secuencia adición-eliminación es la sustitución del grupo unido al grupo acilo por el nucleófilo. De manera superficial pudiera parecer una reacción del tipo SN2, pero el mecanismo es completamente diferente.
Hay que tener en cuenta que en el producto obtenido, el nucleófilo actúa como nuevo grupo del heteroátomo.
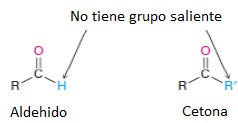
A diferencia de los derivados de acidos carboxílicos, los aldehidos y las cetonas no tienen el grupo con heteroátomo y, por ello, no sufren de sustitución sino de adición. El ion alcóxido intermedio es protonado hasta formar alcohol.

En el caso de los derivados de ácidos, el ion intermedio expulsa el grupo saliente y vuelve a formar el grupo carbonilo.
REACTIVIDAD RELATIVA DE LOS DERIVADOS DE ÁCIDO
La etapa controlante del mecanismo es la adición del nucleófilo al grupo carbonilo, por ello, cualquier efecto que haga el grupo carbonilo más reactivo frente al nucleófilo afectará a la velocidad de reacción. En este sentido se suelen distinguir dos factores: estéricos y electrónicos.
- FACTOR ESTÉRICO
Cuanto más accesible esté el carbono carbonílico al ataque del nucleófilo mayor será la velocidad de la sustitución.
-FACTOR ELECTRÓNICO
La diferencia de reactividad entre los derivados de ácido hay que entenderla en función de las características básicas del grupo saliente. Si es una base débil será un buen grupo saliente y la reacción será rápida. Este el caso de los haluros de acilo, donde el grupo saliente es un haluro. Por el contrario, si el grupo saliente es malo, la reacción será lenta. Este el caso de las amidas, donde el grupo saliente es el amiduro.

Un tioéster es más reactivo que un éster porque el grupo tiolato (RS-) es una base más débil que el brupo alcóxido (RO-). Este hecho impide convertir directamente por sustitución acílica un éster en un tioéster.
Otra manera de explicar la reactividad relativa de los derivados de ácido se basa en el carácter electrofílico del carbono carbonílico de cada uno de ellos. Si el heteroátomo unido a ese carbono es capaz de cederle carga por resonancia, disminuirá la electrofilia del carbono y, por tanto, la tendencia del nucleófilo a unírsele. El nitrógeno de las amidas es un ejemplo de ello. De hecho el enlace C-N tiene un notable carácter doble, por ello, las amidas serían poco reactivas. En el lado contrario nos encontramos con los halógenos.
Una consecuencia de estas diferencias de reactividad es la posibilidad o imposibilidad de convertir unos derivados en otros.

En estos procesos, las principales reacciones que se producen con las siguientes:
Hidrólisis.- Reacción con agua para producir ácido carboxílico
Alcohólisis.- Reacción con alcohol para producir éster
Aminólisis.- Reacción con amoniaco para producir amida
Reducción.- Reacción con hidruro para producir aldehido o alcohol
Reacción Grignard.- Reacción con un organometálico para producir una cetona o un alcohol

HALUROS DE ACILO
PREPARACIÓN
Los haluros de acilo se pueden preparar por reacción de un ácido carboxílico con cloruro de tionilo (SOCl2) o con tribromuro de fósforo (PBr3).

REACCIONES
CONVERSIÓN EN ÁCIDOS CARBOXÍLICOS
La hidrólisis de los haluros de acilo produce ácidos arboxílicos. La hidrólisis es una reacción se sustitución acílica que se inicia con el ataque de la molécula de agua al carbono carbonílico del haluro de acilo. A continuación, el intermedio tetraédrico formado elimina el haluro recuperando el grupo carboxilo y, finalmente, pierde un protón por un ataque básico

Mecanismo de la hidrólisis del cloruro de etanoilo
Como la reacción produce HCl, es necesario llevarla a cabo en presencia de una base como NaOH que lo neutraliza
CONVERSIÓN EN ANHIDRIDO
El ion carboxilato puede actuar como nucleófilo atacando al carbono carbonílico y desplazando al haluro. En este caso se forma un anhidrido de ácido.

CONVERSIÓN EN ÉSTERES
Reacción similar a la hidrólisis y, al igual que ella, debe llevarse a cabo en medio básico (NaOH o piridina) para neutralizar el HCl producido. Es el método habitual de preparar ésteres en laboratorio.

Esta reacción está muy afectada por factores estéricos, siendo más lenta con alcoholes voluminosos. Por ello el orden de reactividad de los alcoles es primario > secundario > terciario.
CONVERSIÓN EN AMIDAS
La reacción de los haluros de acilo con amoniaco o aminas produce amidas, siendo la ruta de síntesis habitual de este tipo de compuestos en el laboratorio. Al igual que la alcohólisis, un aumento en el tamaño del nucleófilo disminuye la velocidad de reacción, por ello, no se produce con aminas terciarias. La producción de HCl obliga a usar exceso de amina o añadir NaOH.

Mecanismo de la síntesis de amidas
CONVERSIÓN EN ALCOHOLES
La reducción de haluros de acilo con hidruros como LiAlH4 produce alcoholes primarios. Esta reacción de reducción ocurre por el mecanismo de sustitución nucleofílica acílica. El ion hidruro ataca al carbono carbonílico produciendo el intermedio tetraédrico que pierde el haluro. El resultado global es la sustitución de un halógeno por un hidrógeno produciendo un aldehido que, seguidamente, es de nuevo reducido por el hidruro hasta alcohol primario.

Los reactivos de Grignard reaccionan con los haluros de acilo para producir alcoholes terciarios con dos sustituyentes idénticos. El mecanismo es similar al de la reducción con hidruro. El reactivo de Grignard se adiciona al haluro de acilo formando el intermedio tetraédrico que, seguidamente, pierde el haluro produciendo una cetona. Inmediatamente, el reactivo de Grignard reacciona con la cetona para producir el alcohol terciario.

ANHIDRIDOS DE ÁCIDO
PREPARACIÓN
Los anhidridos de ácido se suelen preparar mediante la reacción de sutitución nucleofílica acílica de un ácido carboxílico y un ion carboxilato.

REACCIONES
Las reacciones de los anhidridos son similares, pero más lentas, a las de los haluros de acilo. Se hidrolizan con agua para producir ácidos, reaccionan con alcoholes para producir ésteres, con aminas para formar amidas y con hidruros para formar alcoholes.


ÉSTERES
PREPARACIÓN

El método general de obtención de ésteres es un proceso de sustitución nucleofílica acílica que parte de un ácido carboxílico que es transformado en haluro de acilo con cloruro de tionilo. A continuación, el haluro de acilo es tratado con un alcohol en medio básico, normalmente piridina. Como alternativa se puede emplear la esterificación de Fischer. Para ello se parte de un ácido carboxílico y se trata con un alcohol en medio ácido mineral fuerte. Otra opción sería una reacción SN2 entre un ion carboxilato (obtenido al tratar el ácido carboxílico con NaOH) y un haluro de alquilo.
REACCIONES
Los ésteres sufren las mismas reacciones que los demás derivados de ácido, solo que más lentas. Los ésteres pueden ser hidrolizados hasta ácidos carboxílicos en medios ácido o básico. En este último caso a la reacción se le denomina saponificación. La hidrólisis de los ésteres es un proceso de sustitución nucleofílica acílica en el que el ion hidroxilo actúa como nucleófilo atacando el carbono carbonílico y produciendo un intermedio tetraédrico que, inmediatamente, pierde el ion alcóxido y produce un ácido carboxílico que es desprotonado por la base presente presente en el medio.

Mecanismo de la hidrólisis alcalina de ésteres
Los ésteres reaccionan con amoniaco o aminas para producir amidas.

Los ésteres se pueden reducir con hidruros como LiAlH4 para dar alcoholes primarios. El mecanismo es similar al descrito en los haluros de acilo. El ion hidruro ataca el carbono carbonílico provocabdo la salida del grupo alcóxido y produciendo un aldehido que es inmediatamente reducido por el hidruro hasta alcohol.

Los ésteres reaccionan con dos equivalentes de reactivo de Grignard para dar alcoholes terciarios con dos sustituyentes iguales.

AMIDAS
PREPARACIÓN
Las amidas son habitualmente preparadas por reacción entre un haluro de acilo y amoniaco o una amina (primaria o secundaria).

Mecanismo de la formación de etanamida
a partir de cloruro de etanoilo
REACCIONES
Las amidas sufren hidrólisis hasta ácido carboxílico en medios ácido o básico. El proceso es más lento que con haluros de acilo o ésteres pero el mecanismo es semejante. En medio ácido el nucleófilo es agua.

En medio básico el nucleófilo es el ion hidroxilo. En este caso el intermedio tetraédrico tiene que eliminar un ion amiduro, que dada su elevada basicidad es mal grupo saliente. Por ello, la hidrólisis de amidas evoluciona con mayor velocidad en medio ácido.

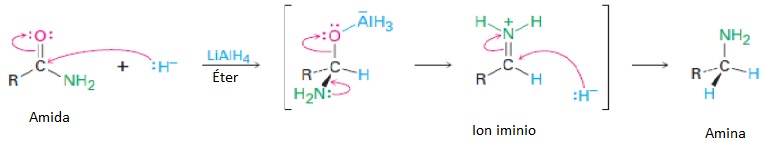
Las amidas pueden ser reducidas por el hidruro LiAlH4, siendo el producto una amina. El efecto neto de la reducción de una amida es la conversión de un grupo carbonilo en un grupo metileno.

El proceso se inicia con el ataque nucleofílico del hidruro al carbono carbonílico, seguido por la expulsión de un átomo de oxígeno como un ion aluminato para dar un ion iminio intermedio que es reducido por el hidruro hasta amina.