ESPECTROSCOPÍA RMN
DESPLAZAMIENTO QUÍMICO
Para obtener espectros RMN a través de la web disponemos de bases de datos:
SDBS
Úselas para obtener los espectros RMN de las siguientes sustancias:
benceno y ácido acético
ESPECTROSCOPÍA: ORIGEN DEL PROBLEMA
ESPECTROSCOPÍA ULTRAVIOLETA-VISIBLE
ESPECTROS IR DE SUSTANCIAS ORGÁNICAS
Benceno
Ácido acético

Una sola señal a 7,33 ppm (RMN 1H)
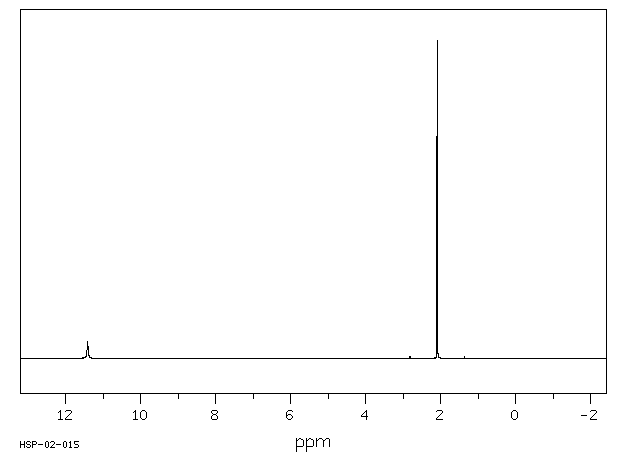
Dos señales una a 2,1 y otra a 11,4 ppm (RMN 1H)
Si todos los protones o los núcleos de carbono de una molécula se comportaran de la misma manera ante la irradiación de radiofrecuencia, se produciría una sola señal RMN con la frecuencia de resonancia (única) y la técnica tendría escaso valor analítico (en todo caso corroborar que en la molécula exitían protones o cúcleos de carbono). Por suerte las cosas no son así.
En el benceno sólo hay una señal, es decir, todos los protones son idénticos, sin embargo, en el ácido acético hay dos señales, por tanto, hay dos “tipos de protones”. Esto no quiere decir que sean de distinta naturaleza o composición, sino que están en un entorno diferente de cara a esta técnica analítica: uno forma parte de un grupo metilo y el otro está unido a un átomo de oxígeno. El entorno eléctrico de ambos protones es muy distinto y al interactuar con el campo magnético externo lo hacen de manera diferente, siendo necesarias diferentes frecuencias de resonancia en cada caso.
Como vemos no todos los protones absorben ondas de radio de la misma frecuencia. El campo magnético creado por las cargas eléctricas (electrones y otros núcleos) que los rodean (H´)se opone al campo magnético externo (Ho) dando lugar a un campo magnético local (HLOC) menor que el aplicado.

Cuanto mayor sea este apantallamiento mayor será el campo magnético o la frecuencia de las ondas de radio a aplicar para que se produzca la resonancia.

Como puede observarse en un espectro RMN se representa la intensidad de la señal frente a la frecuencia de resonancia.
Como la frecuencia de resonancia depende de la intensidad del campo magnético usado, si en el eje horizontal se usara esa frecuencia expresada en Hz, sólo serían comparables los espectros que se realizaran en la misma condiciones experimentales. Para solventar el problema la escala de este eje es relativa:
-
Se ha escogido una sustancia de referencia (en el caso de los protones el tetrametilsilano, TMS). Su señal está a la derecha del espectro y a partir de ella se miden las posiciones a las que aparecen las demás señales.
-
La posición del resto de señales se indica mediante el desplazamiento químico (δ) medido de la siguiente manera:
El numerador es la diferencia de frecuencias entre el TMS y nuestra señal. El denominador es la frecuencia del aparato empleado. Por ejemplo si nuestra señal aparece a 60 Hz del TMS en un aparato de 60 Mhz , el desplazamiento químico sería δ = 1 ppm, es decir una parte por millón de la frecuencia del aparato empleado. Si aparece a 1,3 ppm en un aparato de 200 Mhz es porque nuestra señal lo hace a 260 Hz del TMS.
De esta manera los valores obtenidos en el eje horizontal no dependen del aparato empleado para medirlos y son comparables con los obtenidos en cualquier otro aparato.
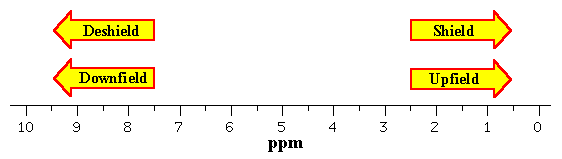
Campo bajo <-----------------> Campo alto
Una señal de 10 ppm está a campo más bajo que otra de 5 ppm
Los desplazamientos químicos más comunes son los siguientes:
Factores que afectan al desplazamiento químico de los protones
Efecto inductivo
Si un átomo más electronegativo retira carga eléctrica que previamente estaba en torno a un protón, el campo local que se oponía al externo disminuye, en consecuencia la resonancia se produce con un campo externo menos intenso. Ojo: En términos de frecuencia diríamos que se produce a mayor frecuencia, más a la izquierda.
existe una relación lineal entre la electronegatividad del sustituyente y el desplazamiento químico del protón
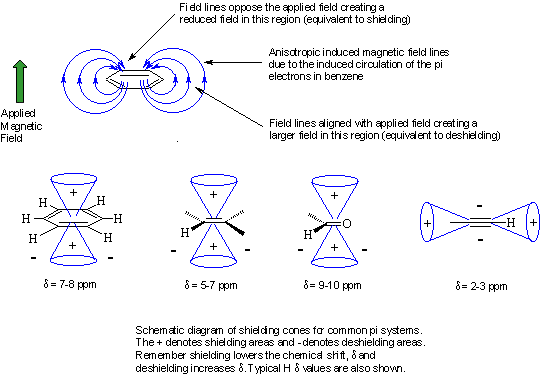
Anisotropía magnética de los sistemas π
Cuando los sistemas de electrones π son sometidos al campo magnético externo inducen un otro campo que se opone al anterior. Dependiendo de las carácterísticas del sistema concreto (aromático, alqueno, carbonilo, ...) se producen en la molécula zonas en las que ambos campos (externo e inducido) tiene el mismo sentido y otras en las que tienen sentidos contrarios. En el primer caso el campo magnético efectivo que sienten los protones aumenta y, por tanto, lo hace la frecuencia de resonancia (resuenan a campo bajo, es el caso de los protones del benceno). En el segundo caso, el campo efectivo al que se ven sometidos los protones es menor y también la frecuencia de resonancia, la señal, por tanto, se desplaza hacia campo alto, hacia la derecha en el espectro (caso de los alquinos).